Aivojen glioomatoosi
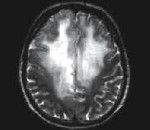
Aivojen glioomatoosi — diffuusi aivojen tunkeutuminen epätyypillisiin gliasoluihin, joka ulottuu yli kaksi aivojen lohkoa. Tyypilliset kliiniset oireet ovat spastinen paresis, progressiivinen kognitiivinen heikkeneminen, epileptisiä kohtauksia, Cephalalgia, pikkuaivosyndrooma, kallon hermojen toimintahäiriö. Tarvittavat diagnostiset testit sisältävät aivojen MRI, elektrokefalogiografia ja aivokuopan biopsia. Hoito toteutetaan yhdistämällä kemoterapia ja aivojen diffuusi säteilytys. Oireellinen hoito suoritetaan samanaikaisesti.
- Aivojen glioomatoosin syyt
- synnyssä
- luokitus
- Aivojen glioomatoosin oireet
- komplikaatioita
- diagnostiikka
- Aivojen glioomatoosin hoito
- Ennuste ja ennaltaehkäisy
Aivojen glioomatoosi

termi «aivojen glioomatoosi» otettiin käyttöön ensimmäisen kerran vuonna 1938. WHO: n vuoden 2007 luokituksen mukaan, aivojen glioomatoosi viittaa astrosyyttisiin neuroepiteelisiin kasvaimiin, neoplasmat, joilla on III asteen maligniteetti. Uudessa luokassa keskushermoston kasvaimia (WHO, 2016 vuosi) aivojen glioomatoosia pidetään hajotetun glioma-levinteen muunnoksena. Neoplasia viittaa harvinaisiin aivokasvaimistoihin. Neurotieteiden kirjallisuudessa esiintymistieto vaihtelee välillä 0,6-8 tapausta vuodessa. Tähän vaikuttaa kaikki ikäryhmät, ihmiset sairastuvat useimmiten 40-60-vuotiaina. Miehet kärsivät glomatoosiin useammin kuin naisilla, suhde on 1,3:1.
Aivojen glioomatoosin syyt
Kasvainten histokemiallinen ja geneettinen tutkimus, yrityksiä on tehty 21-luvun alusta lähtien, sallittiin havaita geneettiset muutokset kasvainsoluissa verrattuna normaaleihin glysoyytteihin. Tunnetuimmat geenimutaatiot IDH1, IDH2, esiintyy 70: ssa% tapauksissa. Mutaatiot aiheuttavat muutoksen biokemiallisissa prosesseissa terveellisen solun sisällä ja sen transformaatiossa tuumorisoluiksi. Etiofaktory, herättävät mutaatioita ja aiheuttavat onkogeneesi, ei ole juuri asennettu. Onkologisen prosessin mahdollinen multifaktorimekanismi, joka käsittää seuraavat komponentit:
- Onkogeeniset tekijät. Todennäköisesti mutageeninen rooli on radioaktiivista säteilyä, onkogeenisiä viruksia (sytomegalovirus, polyomavirus, herpesinfektio), haitallisia kemikaaleja, sisältyvät joihinkin elintarvikkeisiin (säilöntäaineita, väriaineet, emulgointiaineet), saastunut ilma. Nämä vaikutukset voivat aiheuttaa muutoksia solujen geneettisessä laitteistossa, mikä johtaa jälkimmäisen muuttamiseen syöpäsoluiksi.
- immunosuppressio. Kehon immunosuppressiivinen tila kehittyy kortikosteroidihoidon aikana, sytostaatit, pitkäaikaisia kroonisia sairauksia. Se johtaa siihen, ettei kasvainten vastaisia mekanismeja ole aktivoitu, joka on vastuussa muutettavien solujen poistamisesta. Tulos on tuumorisolujen määrän esteetön nousu, progressiivinen kehitys oncoprosessin.
- Geneettinen herkkyys. Geneettisesti määritelty hajoavuus keskushermoston erilaisille onkopatologialle voidaan jäljittää useissa perinnöllisissä sairauksissa (neurofibromatosis, Hippel-Lindau-tauti, Li-Fraumeenin oireyhtymä). Genomiin liittyvän hajoamisen toteutumismekanismeja ei ole vielä määritetty.
synnyssä
IDH1-geenejä/2 koodaavat entsyymejä, katalysoivat reaktiot alfa-ketoglutaraatin synteesiin (pentoosi) ja sen karboksylaatio isosy- traatissa. Näiden geenien mutaatiot johtavat ilmoitettujen biokemiallisten reaktioiden estämiseen, pentoksen muuntaminen on-metaboliitiksi 2-hydroksiglutaraatiksi. Intrasellulaariset dysmetaboliset prosessit aiheuttavat muutoksia normaalien glioyyttien parametreihin, niiden hankkiminen kasvainsolujen ominaispiirteisiin: solutypismi, taipumus hallitsemattomaan jakautumiseen. Muiden mutaatioiden läsnäollessa solun genomissa toteutetaan samanlaisia patogeneettisiä mekanismeja.
Aivojen glukoosimuutos eroaa syöpäsolujen hajakuormituksesta aivokudokseen ilman kasvainsolmujen muodostumista. Pudotus kestää vähintään kaksi lohkoa, jaetaan molemmissa puolipallissa. Useimmiten (76%) tunkeutuva iso aivot, corpus callosum. Puolet tapauksista havaitaan sillan osallistuminen, keskiaivojen. Thalamuskudoksen gliomatoosi havaitaan 43: ssä% tapauksissa, subkorttinen ganglia — klo 34%, pikkuaivot — klo 29%. Aivokuoren tappio on merkitty 19: ssä% sairas. Mikroskooppisesti, glioomatosionin fokaalit edustavat epätyypilliset gliasolut, lähinnä samankaltaisia kuin astrosyytit. Joissakin tapauksissa hallitsevat syöpäsolut, fenotyyppisesti identtiset oligodendroglioyytit.
luokitus
Koska WHO luokittelee aivojen glioomatoosin diffuusi gliooman muodoksi, sen merkitys saadaan sen erottamisesta morfologian fenotyyppisten ominaisuuksien mukaan. Solutyyppitiedot, gomatoosialueen osia, on ensisijainen ennustearvo. Tältä osin on kolme päävaihtoehtoa:
- astrosyyttien. Gliomatoottisia vyöhykkeitä edustavat epätyypilliset astrosyytit. Yleisin tyyppi gliomatosis, on II-III maligniteettiaste. Ajan myötä se voi muuttua enemmän pahanlaatuiseksi glioblastoomamuunnoksi.
- oligodendrogliaalisen. Gliomatoottiset kohteet koostuvat epätyypillisista oligodendroiroyytteistä. Maligniteettiaste — II-III. Tulevaisuudessa mahdollinen glioblastooma kasvaimen rappeuma.
- glioblastooma. Morfologisesti edustavat huonosti erilaistuneet epätyypilliset solut. Toteutuu pääasiassa tai edellisten vaihtoehtojen muuttamisesta johtuen. Aggressiivisin aivojen oncoprosessi, IV maligniteettiaste.
Tuumorisolujen geneettisen testauksen tuominen lääketieteelliseen käytäntöön johti gliomien erottamiseen IDH-mutaation läsnäolon mukaan. Jos havaitaan IDH1-geenivirhe/IDH2-kasvain, joka on luokiteltu IDH-mutaatioksi. Geneettisen analyysin kielteisellä tuloksella kasvainta pidetään villityyppisenä IDH: ksi. Jos IDH-testaus ei ole käytettävissä, kasvain luokitellaan NOS: ksi.
Aivojen glioomatoosin oireet
Oireet ovat erittäin epäspesifisiä, taudin alkuvaiheissa ei heijasta leesion massiivisuutta. Tyypilliset pyramidihäiriöt, dementia. Vaurion hallitseva vaikutus yhdellä pallonpuoliskolla johtaa vastakkaisten ääripäiden hemipareesin kehittymiseen, kahdenvälinen gliomatoosi, joka ilmenee vaihtelevalla tetraparesialla. Lihasheikkouteen liittyy lisääntynyt jänteen refleksejä, spastinen hypertonus, antaen raajojen puoliksi taivutetun asennon. Henkisen pallon rikkomukset ilmentävät muistin vähenemistä, huomio, hidas ajattelu. Kognitiivisen toimintahäiriön jatkuvasti edistyksellinen luonne johtaa amnesian elementtien kehittymiseen, dyskalkulia, agnosia, apraksia, jota seuraa siirtyminen syvään orgaaniseen dementiaan. Mielenterveyshäiriöt ovat mahdollisia: käyttäytymisen muutos, aggressiivisuus, psykomotorinen agitaatio, euforia.
40% potilaat valittavat kepalgiaa, yllään hajanainen. Kallonsisäisen hypertension oireet (pahoinvointia ilman ruokaa, oksentelu cephalgian korkeudella, painovoima silmämökeille) esiintyy kohdassa 34% sairas. B 38% epileptisten paroksysien tapaukset. Samalla taajuudella havaitaan eri aivojen hermojen toimintahäiriöitä. B 33% aivo-glomatoosin esiintyminen aivoinfarktin oireyhtymässä. Merkkejä serebellarin ataksia ovat laajamittainen nystagmus, kävely epävakaus, johon liittyy kehon poikkeama sivulle, discoordination, liikkeen hypermetria, laulettu puhe, makrografiyu. Aistihäiriöitä havaitaan 18: ssä% tapauksissa, jota esittäytyy pinnallisella ja syvähyperestesialla, paresthesias.
komplikaatioita
Bulbar-ryhmän kraniaalisten hermojen tukahduttamiseen liittyy nielemisvaivoja. Ruokinnassa voi olla monimutkainen kouristelu/nestettä hengityselimessä kehitystyössä keuhkokuumeella. Äännetyt pyramidal, sairastavat sairastavat potilaan sänkyä. Moottorin toiminnan rajoittaminen ilman asianmukaista hoitoa on täynnä painehaavan esiintymistä, kongestiivinen keuhkokuume. Spastinen paresis johtaa yhteisten kontraktuurien muodostumiseen. Vakavimmat hengenvaaralliset komplikaatiot ovat mahdollisia aivokuoren tappion takia, missä ovat verisuonis- ja hengityselimet.
diagnostiikka
Diagnoosivaikeudet, jotka liittyvät kliinisen kuvan epäspesifisuuteen. Neurologisessa tilassa määritetään monimuotoinen neurologinen vaje, mikä viittaa aivokudosvaurion hajakuormaan. Ennen neuroimaging-ajanjaksoa aivojen glioomatoosin diagnosoitiin yksinomaan patologit. Taudin moderni intravitaalinen diagnoosi on mahdollista vain aivojen MRI: n ja biopsian tulosten mukaan. Luettelo kyselyistä, jonka neurologi nimeää diagnoosin aikana, se sisältää:
- elektroenkefalografia. EEG suoritetaan alkuperäisessä diagnostisessa vaiheessa. Rekisteröi hajanaisia muutoksia bioelektriseen aktiivisuuteen. Paroksismaattiset epileptogeeniset adheesiot, joita esiintyy kouristuksia aiheuttavan oireyhtymän tapauksessa.
- Magneettinen resonanssikuvaus. T1-tilassa kasvain on iso- tai hypo-intensiivinen, mikä vaikeuttaa sen esiintyvyyden arvioimista. Diagnoosin kultainen standardi on MRI T2-tilassa, joka antaa loogatoottisten vyöhykkeiden hyper-laajamittaisen visualisoinnin. Brain CT ei välttämättä paljasta kasvainta, koska tässä tutkimuksessa gliomatoosi osoittautuu iodosiksi suhteessa normaaliin aivokudokseen.
- Stereotaktinen biopsia. Huolimatta erilaisten glioomatoosien rakenteen heterogeenisuudesta, useimmat kliinikot tarvitsevat biopsiaa. Tuloksena oleva aivomateriaali suoritetaan histologisella tutkimuksella, jonka avulla voit määrittää kasvaimen morfologisen sitoutumisen, arvioida pahanlaatuisuuden astetta.
- IDH-kirjoittaminen. Uusi diagnostinen menetelmä, vähitellen käyttöön neuro-onkologisessa käytännössä. Se toteutetaan geneettisen PCR-diagnostiikan tekniikan mukaisesti. Kirjoittamisen tulokset otetaan huomioon hoidon taktiikan valinnassa, avulla voit tehdä tarkempia ennakoivia oletuksia.
Aivojen glioomatoosi on erotettava useista CNS-lymfoomista, multifokaalinen glioblastooma, aivotulehdus, progressiivinen leukoenkefalopatia. Enkefaliitille on tunnusomaista vastaava epidemiologinen historia, leukoenkefalopatialle — kehitys HIV: n taustalla, JC-viruksen DNA-detektio aivo-selkäydinnesteessä. Erota gloomatoosi multifokalisista leesioista (lymfoomat, glioblastomas) sallii MRI.
Aivojen glioomatoosin hoito
Kasvainprosessin diffuusi luonne ei salli radikaalin kirurgisen hoidon. Toimenpide on mahdollista yhdistämällä gliomatoosi yhdellä suurella fokusoivalla vaurioalueella. Tällaisissa tapauksissa neurokirurgiset toimet pyrkivät poistamaan taudinpurkauksen. Tärkeimmät konservatiivisen hoidon menetelmät ovat:
- Radiologinen hoito. Suoritettiin sarja sädehoitoa, jossa on koko aivosäteily. Paras tulos saadaan IMRT: n avulla — altistuminen tietokoneella varustetuilla röntgenhygiakuomilla. Menetelmällä voit säätää valotuksen voimakkuutta aivojen eri osissa: suora säteily suuriin gliomatoosialueisiin, minimoida kriittisten aivojen rakenteiden säteilyannos.
- kemoterapia. Yhdistetty sädehoidon kanssa. Se toteutetaan asteittaisella kurssilla hoidettaessa sytostaatteja: temotsolomidi, karmustiini, karboplatiini. Useimpien lääkkeiden tehokas käyttö erilaisilla toimintatavoilla. Kemoterapiakurssien välinen tauko johtuu kemoterapiahuumeiden voimakkaasta sivuvaikutuksesta, tarve palauttaa keho.
- Oireellinen hoito. Lähetetään helpottamaan taudin tärkeimpiä oireita, sytostaattisen ja sädehoidon sivuvaikutuksia. Antiemetic syö, kipulääke, antiedematous, psykotrooppisten, epilepsialääkkeitä.
Uusia tehokkaita hoitoja kehitetään jatkuvasti. Lupaavimpia ovat kaksi suuntaa – genetiikan ja biokemian. Geenitekniikan alan tutkimus pyrkii löytämään menetelmiä tuumorisolun genomin muuttamiseksi, kykenevä aiheuttamaan apoptoosia. Syöpäsolujen biokemiallisten ominaisuuksien tutkiminen edellyttää etsimään radikaalisti uusia farmakologisten vaikutusten menetelmiä kasvaimen prosessiin.
Ennuste ja ennaltaehkäisy
Aivojen glioomatoosi — vakava kuolemaan johtava sairaus. Keskimääräinen potilaan elinajanodote diagnoosin jälkeen on 2-3 vuotta, joissakin tapauksissa yli 10 vuotta. Ennuste riippuu morfologisesta variantista, kasvaimen esiintyvyys. Tutkimukset osoittavat merkittävästi potilaan elinajanodotteen kasvua, joilla on glimoja IDH1-mutaatioilla/IDH2, verrattuna potilaisiin, IDH-vapaita kasvaimia. Toimenpiteet gloomatoosin estämiseksi ovat onkogeenisten vaikutusten poissulkeminen, jatkuva virusinfektioiden hoito, säilyttää kunnollinen immuniteetti.
